Compuestos inorgánicos
Se denomina compuesto químico inorgánico a aquellos compuestos que están formados por distintos elementos, pero en los que su componente principal no siempre es el carbono, siendo el agua el más abundante. En los compuestos inorgánicos se podría decir que participan casi la totalidad de elementos conocidos.
Compuestos orgánicos
Es un compuesto químico más conocido como micro molécula o estipula
que contiene carbono, formando enlaces carbono-carbono y carbono-hidrógeno. En
muchos casos contienen oxígeno, nitrógeno, azufre, fósforo, boro, halógenos y
otros elementos menos frecuentes en su estado natural. Estos compuestos se
denominan moléculas orgánicas. Algunos compuestos del carbono, carburos, los
carbonatos y los óxidos de carbono, no son moléculas orgánicas.
-Cloruro de sodio: NaCl
Popularmente denominado sal común, sal de mesa, o en su
forma mineral halita, es un compuesto químico con la fórmula NaCl. El cloruro
de sodio es una de las sales responsable de la salinidad del océano y del
fluido extra celular de muchos organismos. También es el mayor componente de la
sal comestible, es comúnmente usada como condimento y preservativo de comida.
-Cloruro de magnesio: MgCl2
El cloruro de magnesio es un coagulante importante usado en
la preparación de queso a partir de la leche de soja. En algunas zonas del
planeta disminuyó el empleo del cloruro de sodio para evitar la formación de
hielo y aumentó el uso del cloruro de magnesio líquido como anticongelante. El
cloruro de magnesio se ha impuesto como material de almacenamiento de
hidrógeno. El amoniaco (NH3), que es rico en átomos de hidrógeno, se emplea
cómo material intermedio de almacenamiento. Éste pude absorberse con eficacia
sobre el cloruro de magnesio sólido, formando dicloruro de hexamonio (NH4)6Cl2.
El amoniaco es desplazado después por un calor suave y a continuación, se pasa
por un catalizador que lo descompone produciendo hidrógeno.
-Cloruro de hierro: FeCl3
Se utiliza para depurar las aguas residuales y para
tratamiento de agua de consumo. El cloruro de hierro (III) se usa en el
laboratorio como ácido de Lewis para reacciones de catálisis tales como
coloración y reacción de Friedel-Crafts de compuestos aromáticos.
-Carbonato de calcio: CaCO3
El carbonato de calcio puro existe en dos formas
cristalinas: la calcita, de forma hexagonal, la cual posee propiedades de
birrefrigencia, y la aragonita, de forma romboédrica. Los carbonatos naturales
son los minerales de calcio más abundantes. El espato de Islandia y la calcita
son formas esencialmente puras de carbonato, mientras que el mármol es impuro y
mucho más compacto, por lo que puede pulirse. Tiene gran demanda como material
de construcción.
El cloruro de calcio se encuentra en numerosos productos en
forma de gránulos, copos, soluciones y polvos. Es utilizado por los
consumidores, así como en la fabricación, la industria y la medicina. El
cloruro de calcio se encuentra en muchos productos que puedes usar todos los
días.
Se han empleado para el hemoperitoneo diferentes tipos de
gases, desde aire, nitrógeno, argón, helio, CO2 y óxido nitroso. Cada uno de
ellos reviste características distintas, pero en términos generales sólo los
gases solubles (CO2 y N2O) tienen aplicaciones en la práctica de la
laparoscopía. El óxido nitroso es útil en las siguientes circunstancias:
procedimientos diagnósticos, donde no haya necesidad de fulgurar (aunque no es
combustible, sí es comburente y por ello es posible la inflamabilidad sobre
todo si coexiste con otros gases como el hidrógeno y el metano que se producen
en el tracto intestinal), además no hay que olvidar que, en caso de embolismo
aéreo y N2O, el tamaño del émbolo es mayor que con el CO2. Una ventaja reportada
parece ser que el pneumoperitoneo resulta menos doloroso y es factible su
realización bajo anestesia local y sedación.

-Óxido nítrico: NO
Entre las funciones más importantes que cumple el óxido
nítrico en el organismo, cabe mencionar el efecto modulador del tono vascular,
radiotransmisor central y periférico, inmunológico y la agregación plaquetaria.

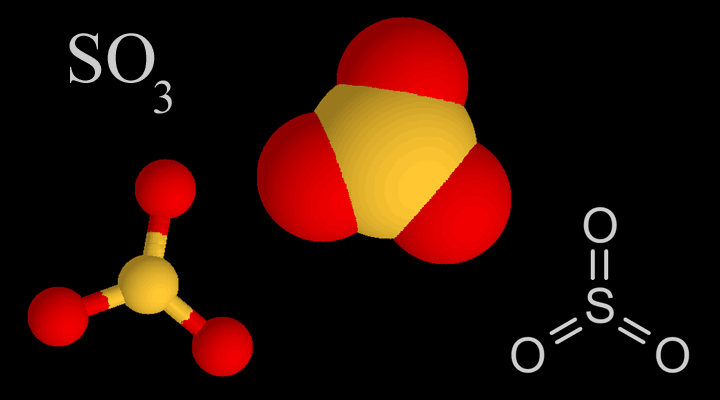
-Óxido de azufre: SO3
Aparte de su papel como intermedio en la fabricación del
ácido sulfúrico el óxido de azufre (IV) es empleado en varias otras síntesis.
Con el cloro da el cloruro de sulfuril (SO2Cl2), un importante intermedio en la
industria química. Si se hace reaccionar con el cloro y compuestos orgánicos se
pueden obtener en una reacción de clorosulfonación directa, los clorosulfonatos
como precursores de detergentes y otras sustancias. En estado líquido es un
buen disolvente y es utilizado como tal. En la industria alimenticia se aplica
como conservante y antioxidante sobre todo para zumos, frutos secos,
mermeladas, vino etc.
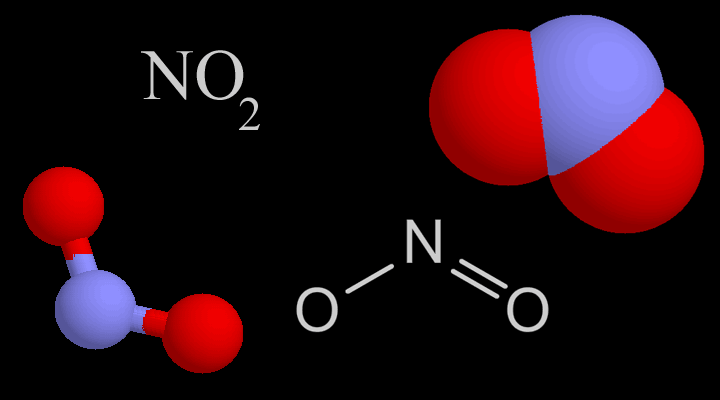
-Óxido de nitrógeno: NO
El monóxido de nitrógeno es el producto primario de la
combustión catalítica del amoniaco mediante el método de Ostwald y, por lo
tanto, un intermediario importante en la producción del ácido nítrico (HNO3).
En el laboratorio se genera más convenientemente por reacción de ácido nítrico
diluido con cobre, si los otros productos posibles de la reacción como el
dióxido de nitrógeno no molestan o pueden ser eliminados (por ejemplo, por
absorción en agua). Se usa para detectar radicales en la superficie de polímeros.
-Oxido de aluminio: Al2O3
Dada su gran dureza y elevado punto de fusión el óxido de
aluminio suele utilizarse como:
Aislante térmico.
Dispositivo refractario.
Esmaltes y Cerámicas (proporciona dureza)
-Oxido de plata: AgO2
Existen diversos usos en los que se utiliza el óxido de
plata, como por ejemplo:
Medicina: generalmente usado en uso externo dado su alta
toxicidad.
Electricidad: en generadores eléctricos.
Electrónica: usado en contactos de circuitos.
Joyería: en la realización de artículos ornamentales.
Química orgánica: usado como un agente oxidante.

Excelente informacion muy interesante y practica .gracias por compartirla
ResponderEliminar